10月31日、ファイザー株式会社は、「手術不能又は再発乳癌」の効能・効果で、サイクリン依存性キナーゼ(CDK)4/6阻害薬パルボシクリブ(米国商品名イブランス;IBRANCE)の国内における製造販売承認申請を行ったと発表した。
パルボシクリブは、世界初の経口CDK4/6阻害薬であり、米国食品医薬品局(FDA)により2013年4月にブレークスルー・セラピー(画期的治療薬)の指定を受け、2015年2月に迅速承認され、既に世界20カ国以上で承認されている。
現在の米国における適応症は、「ホルモン受容体陽性/HER2陰性の閉経後進行または転移乳がんに対する初回内分泌療法(レトロゾールとの併用)」および「内分泌療法により疾患が進行したホルモン受容体陽性/HER2陰性の進行または転移乳がん(閉経の有無を問わない)に対する治療(フルベストラントとの併用)」となる。
目次
標準的なホルモン療法にパルボシクリブを併用した2つの試験結果による申請
今回、日本も参加した2つの国際共同第3相試験(PALOMA-2とPMLOMA-3)、および海外/国内第Ⅱ相試験の結果、パルボシクリブは進行乳がんに対して内分泌療法との併用にて臨床的に意義のある有効性が認められ、これらの結果を取りまとめ、今回の申請に至ったとのこと。
PALOMA-2試験は、エストロゲン受容体陽性/HER2陰性の閉経後進行乳がん患者666名を対象に、初回内分泌療法としてパルボシクリブとレトロゾール併用を検討したもの。プラセボとレトロゾール併用投与群と比較して、パルボシクリブとレトロゾール併用投与群において有意な無増悪生存期間(PFS)の延長が認められた。PFS中央値はパルボシクリブとレトロゾール併用投与群で24.8カ月、プラセボとレトロゾール併用投与群で14.5カ月であった。
閉経後ホルモン受容体陽性HER2陰性乳がん レトロゾールとパルボシクリブの併用療法の有効性を示唆 ASCO2016(オンコロニュース20160613)
PALOMA-3試験は、内分泌療法を受け疾患進行を認めたホルモン受容体陽性/HER2陰性の進行乳がん患者(閉経の有無を問わない)521名を対象に、パルボシクリブとフルベストラント併用を検討したもの。プラセボとフルベストラント併用投与群と比較して、パルボシクリブとフルベストラント併用投与群において有意な無増悪生存期間(PFS)の延長が認められ、中間解析の結果、試験は有効中止となっている。PFS中央値はパルボシクリブとフルベストラント併用投与群で9.2カ月、プラセボとフルベストラント併用投与群で3.8カ月であった。
進行乳がん2次治療 パルボシクリブとフルベストラント併用 QOLも改善 ECC2015(オンコロニュース20151006)
乳がん 細胞分裂を制御する薬剤パルボシクリブが有効 がん進行抑制期間2倍に ASCO2015(オンコロニュース20150614)
CDK4/6阻害薬 パルボシクリブとは
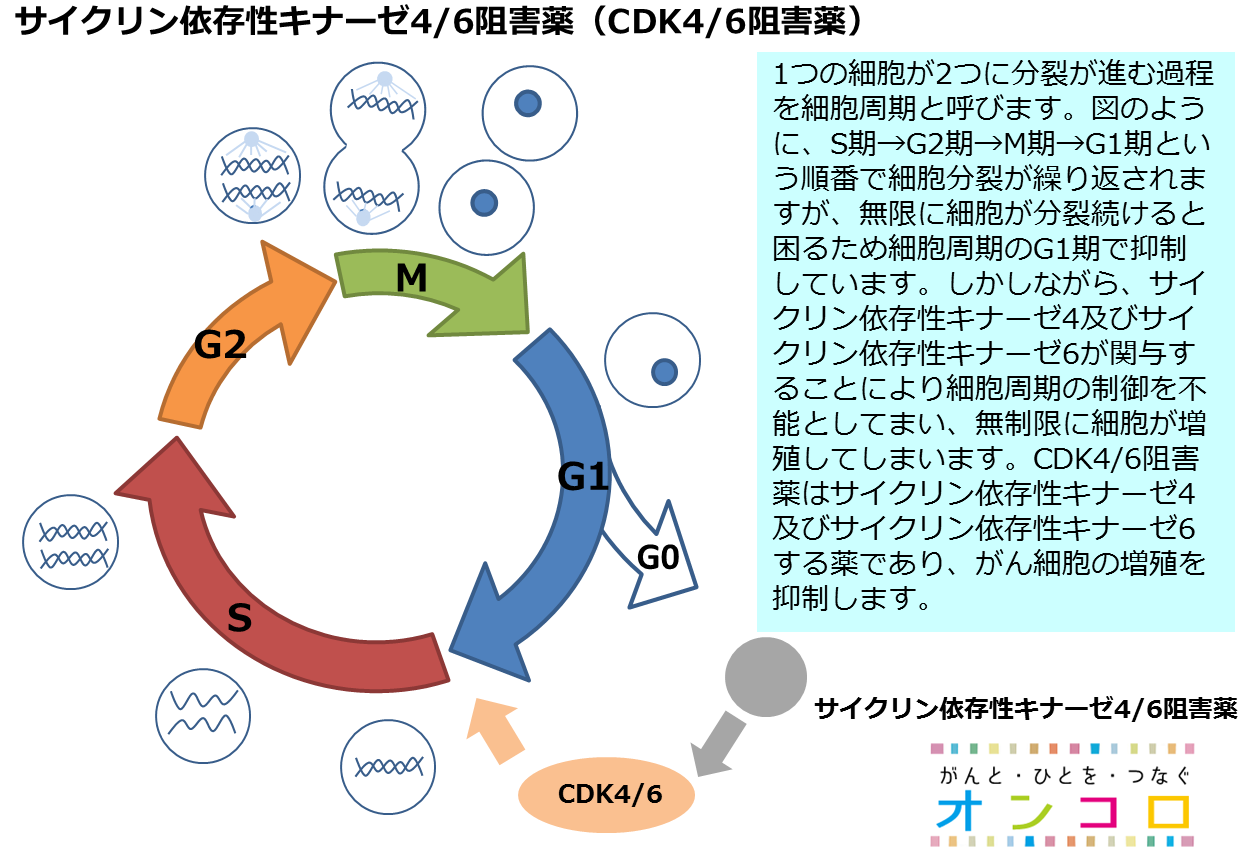
パルボシクリブは、サイクリン依存性キナーゼ(CDK)4/6を阻害する新規の経口分子標的薬である。CDK4/6は、細胞周期の調節に主要な役割を果たしており、細胞増殖を引き起こす。パルボシクリブはCDK4および6を選択的に阻害して、細胞周期の進行を停止させることにより、腫瘍の増殖を抑制すると考えられている。
記事:可知 健太
この記事に利益相反はありません。


