■この記事のポイント
・切除不能な進行・再発の非小細胞肺がんに対して、オプジーボが承認。
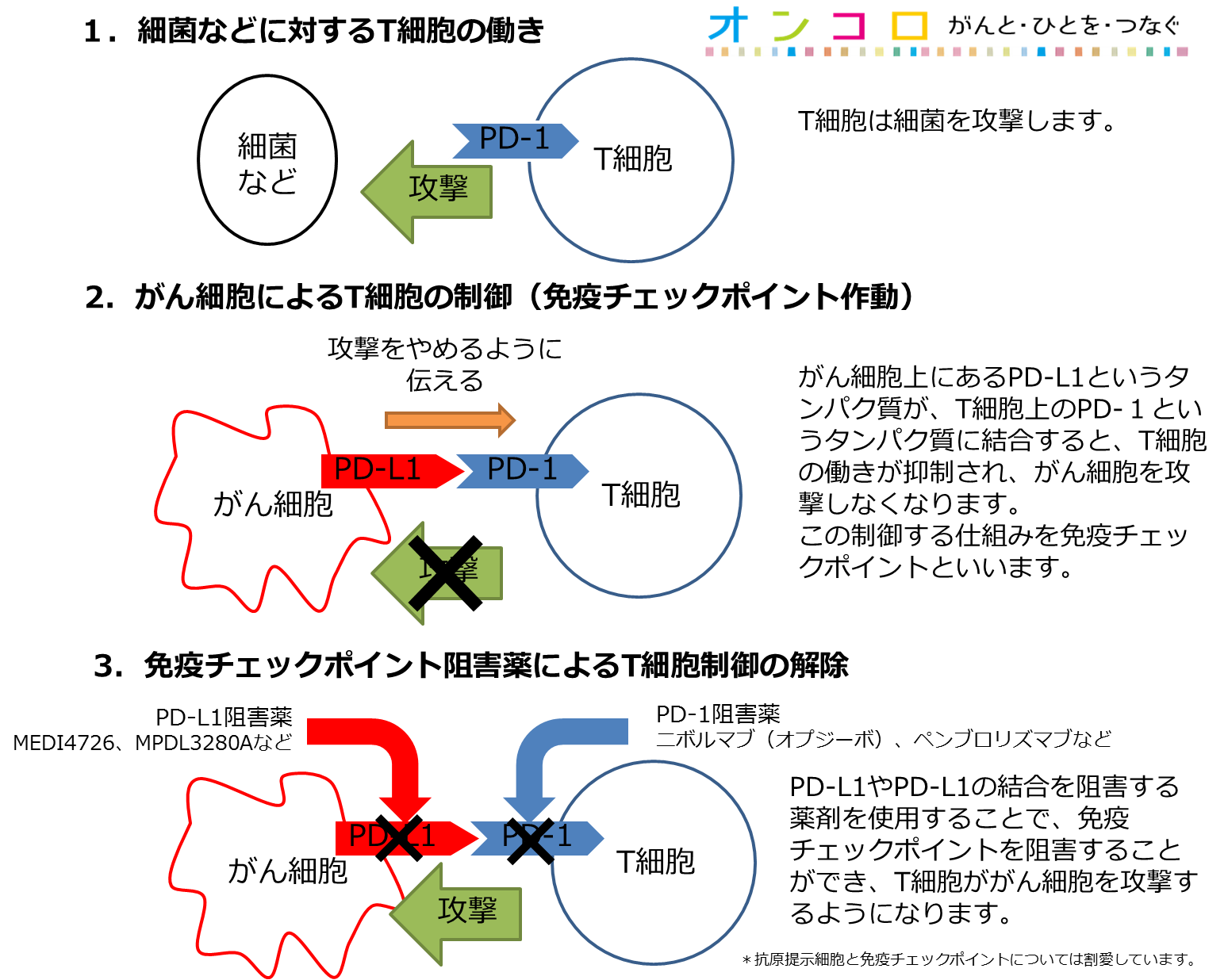
・がん細胞の免疫機構を制御するメカニズムを阻害する薬剤。
・効果がある人と効果がない人がわかっていないこと、安全性への懸念点、薬剤費用など課題は残る。
12月17日、の小野薬品工業はニボルマブ(商品名オプジーボ)の「切除不能な進行・再発の非小細胞肺がん」に関する効能・効果に係る製造販売承認事項一部変更承認取得したと発表しました。
オプジーボは、化学療法の治療歴を有する進行期非小細胞肺がんの患者さんの全生存期間の延長を世界で初めて示した、PD-1 とPD-1 リガンドの経路を阻害する免疫チェックポイント阻害剤となります。
非小細胞肺がんに関する、オプジーボの臨床試験の簡易結果は以下の通りです。
◆進行期肺扁平上皮がんの患者を対象にした海外の第3相臨床試験(CheckMate-017)
・標準治療(ドセタキセル)と比較して、死亡リスクを41%低減
・全生存期間の中央値:オプジーボ群が9.2 カ月、ドセタキセル群が6.0 カ月
・1 年生存率:オプジーボ群が42%に対して、ドセタキセル群が24%
◆進行期非扁平上皮非小細胞肺がんの患者を対象にした海外の第3相臨床試験(CheckMate-057)
・標準治療(ドセタキセル)と比較して、死亡リスクを27%低減
・全生存期間の中央値:オプジーボ群が12.2 カ月、ドセタキセル群が9.4 カ月
・1 年生存率:オプジーボ群が51%に対して、ドセタキセル群が39%
◆肺扁平上皮がんを対象の患者をとした国内の第Ⅱ相試験(ONO-4538-05試験)
・奏効率(一定以上腫瘍を縮小させた方の割合):25.7%
◆国内非扁平上皮非小細胞肺がんの患者を対象とした国内の第Ⅱ相試験(ONO-4538-06 試験)
・奏効率(一定以上腫瘍を縮小させた方の割合):19.7%
小野薬品工業プレスリリース
ブリストルマイヤーズのプレスリリース
オプジーボは効果が期待されている薬剤である一方、以下の問題が残されていることもご留意ください。
・誰に効果があるかがわかっていない(効果がある方がいる一方、効果がない方もいらっしゃること)
・日本人の肺がん患者に対しての安全性が確立されていないこと。
・体重60㎏の方が本薬剤を使用するときの費用は1か月あたり300万円かかること。
これらについては、今後、オンコロでも言及していく予定です。
上記に関するオンコロ上の関連記事は以下の通りです。
オプジーボ使用における保険制度上の課題解決へ 肺癌学会と患者連絡会 要望書提出(オンコロニュース15/12/14)
非扁平上皮非小細胞肺がん ニボルマブ(オプジーボ) 生存期間延長 ASCO2015(オンコロニュース15/6/2)
扁平上皮非小細胞肺がん オプジーボ 長期フォローアップ結果 WCLC2015(オンコロニュース15/9/8)
記事:可知 健太


