5月3日、ランセットオンコロジー( Lancet Oncology )にて、いくつかの進行固形がん患者を対象とした免疫チェックポイント阻害薬抗PD-1抗体ペムブロリズマブ(米国商品名キイトルーダ/キートルーダ)の第1b相臨床試験(KEYNOTE-012試験)の結果が掲載されました。なお、この試験には、アジアから日本、韓国および台湾が参加しており、この文献の主要著者は愛知県がんセンターの室 圭医師となります。
この試験は、進行胃がん、トリプルネガティブ乳がん、尿路上皮がん、頭頸部がんを対象としていますが、今回の報告は進行胃がんにフォーカスされています。
目次
進行胃がんにおける有効性を示唆 日本では先駆け審査指定済み
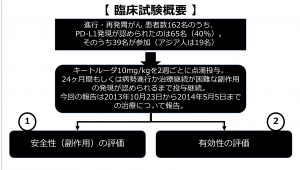
試験概要
この試験には、化学療法を実施した進行胃がん患者にて、PD-L1発現が認められた患者39名を対象にキートルーダを2週間に1度、10mg/kgにて点滴投与した。
参加した患者の背景は以下の通りであり、アジア人が多く参加した試験と言える。
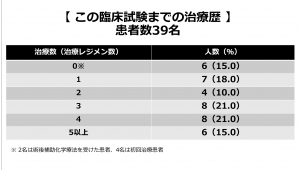
参加したこの試験に参加するまでの治療数と治療薬は以下の通り。
効果に関する結果
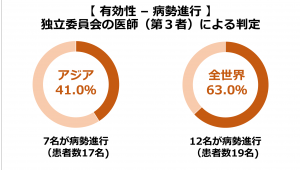
アジア人では、24%の方の腫瘍が一定以上縮小(奏効率24%)。
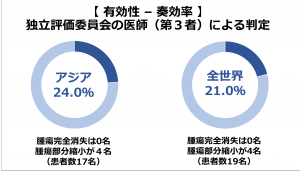
なお、効果が現われるまでの中央値は8週間、奏効期間(効果が持続した期間)の中央値は40週間であった。
また、PD-L1発現量が高いほど効果がある傾向が認められ、一旦、腫瘍が増大してから縮小が得られる患者も認められた。
その一方、アジア人では、41%の方に対して効果を発揮できなかった。
その他、腫瘍の進行を抑えた期間の中央値は1.9か月、生存期間の中央値は11.4か月だった。
(ただし、統計学的に確定していない)
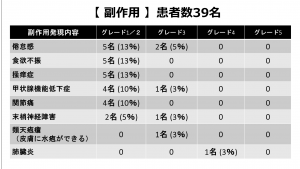
安全性に関する結果
有害事象(副作用)については、今まで報告されている臨床試験と大きい違いは認められていないが、1名の方に重度の肺臓炎が発現している。
まとめ
◆ 第1b試験の結果ではあるが、進行胃がんに対してキートルーダは期待できる有効性と許容できる安全性が示唆されるものでした。
◆ 副作用発現では、倦怠感、甲状腺機能低下症、末梢神経障害、類天疱瘡でそれぞれ1名ずつグレード3、そして肺臓炎は1名グレード4が
認められた。
◆ 効果が期待できる一方、他のがん種と同じく効果が乏しい患者も数多く存在する
なお、進行胃がんに対して、ペムブロリズマブは、初回治療から3次治療まで広く開発されており、また、日本において早期から開発が試みられていることを重視して、PMDAにより先駆け審査指定されています。
参考:ペムブロリズマブ(胃がん)、ASP2215(急性骨髄性白血病)が先駆け審査に指定(オンコロニュース2015/10/28)
その他
【参考】
Pembrolizumab for patients with PD-L1-positive advanced gastric cancer (KEYNOTE-012): a multicentre, open-label, phase 1b trial.(Lancet Oncol. 2016 May 3. pii: S1470-2045(16)00175-3. doi: 10.1016/S1470-2045(16)00175-3.)
Study of Pembrolizumab (MK-3475) in Participants With Advanced Solid Tumors (MK-3475-012/KEYNOTE-012)(NCT01848834)
【日本で実施中の試験】
再発又は転移性の胃腺癌又は食道胃接合部腺癌の患者を対象としたMK-3475の単独療法とシスプラチンと5-フルオロウラシルとの併用療法の第II相試験(KEYNOTE-059)(オンコロ内)
プラチナ製剤及びフッ化ピリミジン系製剤による1次化学療法を受け疾患進行が認められた進行性胃腺癌又は食道胃接合部腺癌の患者を対象としたMK-3475とパクリタキセルを比較する非盲検無作為化第III相試験(KEYNOTE-061)(オンコロ内)
記事:前原 克章・可知 健太
キーワード pembrolizumab Keytruda ペンブロリズマブ 免疫チェックポイント阻害剤
リサーチのお願い
この記事に利益相反はありません。