プログラム細胞死受容体1(PD-1)標的抗体の免疫チェックポイント阻害薬ペムブロリズマブ(商品名キイトルーダ)は、PD-1リガンドであるPD-L1発現陽性を確認した切除不能の進行・再発非小細胞肺がん(NSCLC)の適応で承認されている。抗腫瘍免疫にかかわる分子インドールアミン2,3-ジオキシゲナーゼ1(IDO1)を標的とする経口用阻害薬epacadostat(INCB024360)を併用投与することで、PD-L1の発現レベルにかかわらず奏効が得られることが報告された。2017年6月2日から5日に開催された米国臨床腫瘍学会(ASCO2017)で、第1/2相試験(ECHO-202、KEYNOTE-037、NCT02178722)の最新データが発表された。なお、その他の固形がん(頭頸部扁平上皮がん、腎細胞がん、尿路上皮がん、トリプルネガティブ乳がん、卵巣がん)に対する最新データも発表されたが、別で報じることとする(コチラ)。
目次
複数がん種を対象にがん免疫療法薬としてのepacadostatの有用性を評価するECHOプログラム
IDO1阻害薬epacadostatについて、がん併用療法の中心的役割を担うに足る有効性と安全性を証明できるかどうかが、ECHO臨床試験プログラムで検討されている。その中で、ECHO-202は非小細胞肺がん(NSCLC)や尿路上皮がん(UC)、トリプルネガティブ乳がん(TNBC)といった固形がんのほか、リンパ腫など血液がん患者も対象にキイトルーダとの併用療法を評価する第1/2相試験である。
ECHO-202ではPD-1標的抗体、または細胞傷害性Tリンパ球抗原4(CTLA4)標的抗体を用いたがん免疫療法の経験がある患者を除外して登録し、第1相の用量漸増パート(epacadostat 25mg、50mg、100mg、または300mgを1日2回経口投与)、第1相用量拡大パート(epacadostat 50mg、100mg、または300mgを1日2回経口投与)の登録は終了した。キイトルーダは、増量パートで2mg/kg、拡大パートで200mgを3週ごとに静脈内投与した。
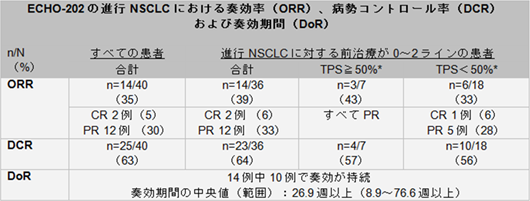
その結果、進行NSCLCの有効性解析対象40例で全奏効率35%(14/40例)が得られ、14例のうち完全奏効(CR)は2例(5%)、部分奏効(PR)は12例(30%)で、病勢安定(SD)の11例を含めた病勢コントロール率(DCR)は63%(25/40例)であった。解析時点で、奏効の14例中10例の奏効が持続し、奏効持続期間(DoR)の中央値は26.9週を超える見込みである。
腫瘍細胞PD-L1発現レベルで分けた層別解析
治療歴が2療法以下で、腫瘍細胞のPD-L1発現レベルを特定した25例中、PD-L1発現陽性細胞の割合が50%以上であった7例の奏効率は43%(3/7例)で(全3例がPR)、SDを含めたDCRは57%(4/7例)であった。50%未満であった18例の奏効率は33%(6/18例)で(CR 1例、PR 5例)、SDを含めたDCRは56%(10/18例)であった。
安全性はすでに報告された第1相試験や他のがん種の患者を対象とする第1/2相試験、あるいはキイトルーダ単独療法のデータと一致し、本併用療法で新たに表出した問題は認められなかった。グレード3以上の有害事象は、主にリパーゼ上昇(3例)、倦怠感(2例)、および発疹(2例)で、有害事象を理由とする治療中止率は5%であった。
トリプトファンの代謝酵素IDO1ががん免疫療法の新たな標的の可能性
がん細胞は、正常細胞とは異なる環境、例えば低酸素状態など特殊な環境に適応して活動する能力を獲得している。生存や増殖を維持するためには、がん細胞の糖代謝や脂質代謝、これらに関連するアミノ酸の代謝は環境に対応して再構築されることが近年わかってきた。実際、がん細胞ではトリプトファンやグルタミン、セリン、グリシンといったアミノ酸の消費ががん種によらず共通して高く、アミノ酸の代謝物を利用して細胞間で連絡し、宿主の抗腫瘍免疫を回避する戦略をとっている。
IDO1はアミノ酸のトリプトファンをキヌレニンに代謝する酸素添加酵素で、免疫担当細胞である樹状細胞に発現するIDO1は制御性T細胞(Treg)を誘導して免疫寛容をもたらし、また、悪性腫瘍に高発現するIDO1はエフェクター細胞やナチュラルキラー(NK)細胞を不活化することで、抗腫瘍免疫を回避させる。こうした免疫回避を主導するのは、IDO1による働きで産生されるトリプトファンの代謝産物キヌレニンと考えられている。IDO1を阻害することによる抗腫瘍活性のメカニズムは不明な点も多いが、動物モデルを用いた研究結果に基づきIDO1を標的とする新薬の開発が始まった。トリプトファンに由来するキヌレニンの産生には、IDO1以外の酵素もかかわることもわかっており、体内で合成することができない必須アミノ酸であるトリプトファンの役割、消費亢進でトリプトファンが欠乏した際の細胞間のネットワーク、細胞へのキヌレニンの働きかけなど、様々な側面からの研究課題は多い。
記事:川又 総江 & 可知 健太
リサーチのお願い
この記事に利益相反はありません。