・リムパーザ、相同組換え修復関連遺伝子変異を有する患者の病勢進行または死亡のリスクを51%低減
・バイオマーカーにより選択された前立腺がん患者の標的治療を検討し、良好な結果が得られた最初の第III相試験
・リムパーザは、BRCA1/2またはATM遺伝子変異陽性の転移性去勢抵抗性前立腺がん患者の無増悪生存期間を2倍以上に延長
目次
転移性去勢抵抗性前立腺がん患者387例を対象とした第III相PROfound試験結果
2019年9月30日、英アストラゼネカ社(以下、アストラゼネカ)および米MSD社(米国およびカナダではMerck社、以下MSD)は、相同組換え修復関連遺伝子変異陽性(HRRm)で、新規ホルモン薬(アビラテロン酢酸エステルまたはエンザルタミドなど)による前治療中に病勢進行が認められた転移性去勢抵抗性前立腺がん(mCRPC)患者387例を対象にオリパラブ(商品名:リムパーザ、以下 リムパーザ)の有効性と安全性を評価した第III相PROfound試験の詳細な結果を発表した。
本試験は、HRRmを有する患者を2つの患者集団に分けて組み入れ解析するよう設計された。主要な解析対象集団は、BRCA1/2またはATM遺伝子変異を有する患者を含めた集団であり、この集団でリムパーザが臨床的ベネフィットを示した場合、副次的な解析対象集団として、HRR関連遺伝子(BRCA1/2、ATM、CDK12およびその他11のHRR関連遺伝子)変異を有する全患者を含めた集団も対象に検定を用いた解析を実施した。
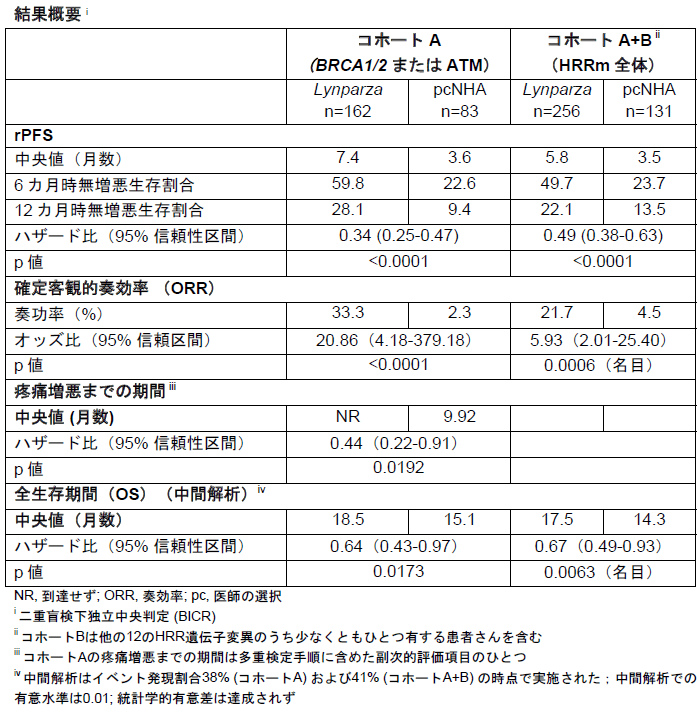
その結果、主要評価項目である画像診断に基づく無増悪生存期間(rPFS)のリムパーザによる統計学的に有意かつ臨床的に意義のある延長が示された。BRCA1/2遺伝子またはATM遺伝子変異を有するmCRPC患者のrPFS中央値は、アビラテロン酢酸エステルまたはエンザルタミド投与群で3.6ヶ月であったのに対し、リムバーザ投与群では7.4ヶ月に延長した。リムパーザはこれら患者の病勢進行あるいは死亡リスクを66%低減した(ハザード比0.34に相当)。
本試験では、主要な副次的評価項目である全HRRm患者集団におけるrPFSも達成した。リムパーザは病勢進行または死亡のリスクを51%低減し(ハザード比0.49に相当)、rPFSの中央値はアビラテロン酢酸エステルまたはエンザルタミド投与群の中央値3.5ヶ月に対し、リムパーザ投与群では中央値5.8ヶ月であった。
本結果はスペインのバルセロナで開催された2019年欧州臨床腫瘍学会(ESMO)の年次総会プレジデンシャルシンポウムにおいて発表された。(抄録 #LBA12_PR)
また、本結果により、中間解析の時点で別の主要な副次的評価項目である2つの患者集団における全生存期間(OS)の改善傾向が示された。この中間解析の時点で、アビラテロン酢酸エステルまたはエンザルタミド投与群で病勢進行が認められた患者の81%が病勢進行後にリンパーザをクロスオーバーして投与していたにも関わらず、BRCA1/2遺伝子またはATM遺伝子変異を有するmCRPC患者のOSの中央値はアビラテロン酢酸エステルまたはエンザルタミド投与群の15.1ヶ月に対し、リムパーザ投与群では18.5ヶ月に延長した。この中間解析の時点で、OSに関する同様の結果が全HRRm患者集団においても認められ、アビラテロン酢酸エステルまたはエンザルタミド投与群ではOSの中央値が14.3ヶ月に対しリムパーザ投与群では17.5ヶ月であった(イベント発現割合41%の時点での解析)。
PROfound試験のリムパーザの安全性および忍容性プロファイルは以前の臨床試験で認められたプロファイルと一貫するものであった。発現率が20%以上の有害事象は貧血(47%)、悪心(41%)、疲労/無力(41%)、食欲減退(30%)、および下痢(21%)。CTCAEグレード3以上の有害事象は、貧血(22%)、肺塞栓(4%)、疲労/無力症(3%)、嘔吐(2%)、呼吸困難(2%)、尿路感染(2%)、食欲減退(1%)、下痢(1%)および背部痛(1%)。リムパーザ投与群の患者の16%が有害事象により投与を中止した。
アストラゼネカとMSDはリムパーザをアビラテロン酢酸エステルとの併用療法でmCRPCの1次治療として評価するために実施中の第III相PROpel試験など、前立腺がんに関する臨床試験を今後も実施していく予定。
※転移性去勢抵抗性前立腺がん(mCRPC)に対するリムパーザの適応は未承認
PROfound試験について
PROfound試験は前向き多施設共同無作為化非盲検の第III相試験で、新規ホルモン薬による前治療に対して病勢進行し、BRCA1/2、ATM、CDK12などの相同組換え修復(HRR)に関連する15の遺伝子のうちのいずれかに変異が認められるmCRPC患者を対象にリムパーザの有効性と安全性を評価する試験。
転移性去勢抵抗性前立腺がん(mCRPC)について
前立腺がんは男性において2番目に罹患率が高いがんであり、2018年には世界中で推定130万人が新たに診断され、高い死亡率を伴う
HRR(相同組換え修復)遺伝子変異について
HRRは二本鎖切断および鎖間架橋の形で損傷したDNAを高い精度でかつ誤りのない修復を可能にするDNA修復プロセス4,5。DNAの損傷を正確に修復できない場合、ゲノムの不安定性につながり、がんの発症原因になります5。HRRの欠損は損傷したDNAを修復する能力の低下につながり、リムパーザなどのPARP阻害剤の標的となるがん細胞の特徴である。PARP阻害剤はDNA一本鎖切断に結合するPARPを捕捉し、複製フォーク停止と崩壊を惹起することで、DNA二本鎖切断を起こしがん細胞死を誘導する4。
リムパーザについて
リムパーザは、ファーストインクラスのPARP阻害剤であり、BRCA1および/またはBRCA2遺伝子変異などの相同組換え修復(HRR)の欠損を有する細胞/腫瘍のDNA損傷応答(DDR)を阻害する最初の標的治療薬。リムパーザによるPARP阻害はDNA一本鎖切断に結合するPARPを捕捉し、複製フォーク停止と崩壊を惹起することで、DNA二本鎖切断を起こしがん細胞を死滅させる。リムパーザはDDR経路に異常をきたした一連のPARP依存性のがん腫に対して開発が進行中。
リムパーザは、現在EU内の国を含む64ヶ国で、BRCA遺伝子変異の有無にかかわらず「プラチナ製剤感受性の再発卵巣がんにおける維持療法」の適応症で承認されている。また、米国、EU、日本、およびその他数の国において、「プラチナ製剤ベースの化学療法で奏効が維持されているBRCA遺伝子変異陽性進行卵巣がんにおける初回維持療法」の適応症で承認を受けている。さらに、米国、日本を含む43ヶ国では、「化学療法後の生殖細胞系列のBRCA遺伝子変異陽性かつHER2陰性の転移性乳がん」の適応症で承認を受けており、EUではこの適応に加えて「化学療法後のBRCA遺伝子変異陽性かつHER2陰性の局所進行性乳がん」の適応症でも承認を受けている。その他の国においても、卵巣がん、乳がん、膵がんに対する適応症について、規制当局による審査が進行中。
アストラゼネカおよびMSDが共同で開発と商業化を行っているリムパーザは、進行卵巣がん、転移性乳がんの適応症で承認を受け、世界中で2万5千人以上の患者に使われている。また、リムパーザに対しては、PARP阻害剤のなかでも幅広く最も進んだ臨床試験開発プログラムが行われている。アストラゼネカとMSDは協業して、リムパーザが様々ながんのタイプにわたり、単独療法および併用療法で、複数のPARP依存性腫瘍に及ぼす影響を解明しようとしている。
出典
1. Bray, F., Ferlay, et al. (2018). Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: A Cancer Journal for Clinicians, 68(6), pp.394-424.
2. Cancer.Net. (2019). Treatment of metastatic castration-resistant prostate cancer. [Accessed September 2019].
3.Cancer.Net. (2019). Prostate Cancer – Statistics. [Accessed September 2019].
4.Li, X. and Heyer, W. (2008). Homologous recombination in DNA repair and DNA damage tolerance. Cell Research, 18(1), pp.99-113.
5. Ledermann, J., Drew, Y. and Kristeleit, R. (2016). Homologous recombination deficiency and ovarian cancer. European Journal of Cancer, 60, pp.49-58.
参照元:
2019年10月7日発行アストラゼネカ株式会社プレスルーム
この記事に利益相反はありません。


