講演タイトル:『肺がん(小細胞肺がん)』
演 者:中川 和彦 先生(近畿大学病院 腫瘍内科部門臨床腫瘍内科)
日 時:9月27日(金)
場 所:日本橋ライフサイエンスハブ8F D会議室
今月は、小細胞肺がんをテーマにご来場頂きました。
クローズドセミナーであるため全ての情報は掲載できませんが、ポイントとなる情報をお伝えしていきます。
今回は「小細胞肺がんの基礎知識、限局型小細胞肺がんについて、進展型小細胞肺がんについて」を中心にご講義頂きました。
目次
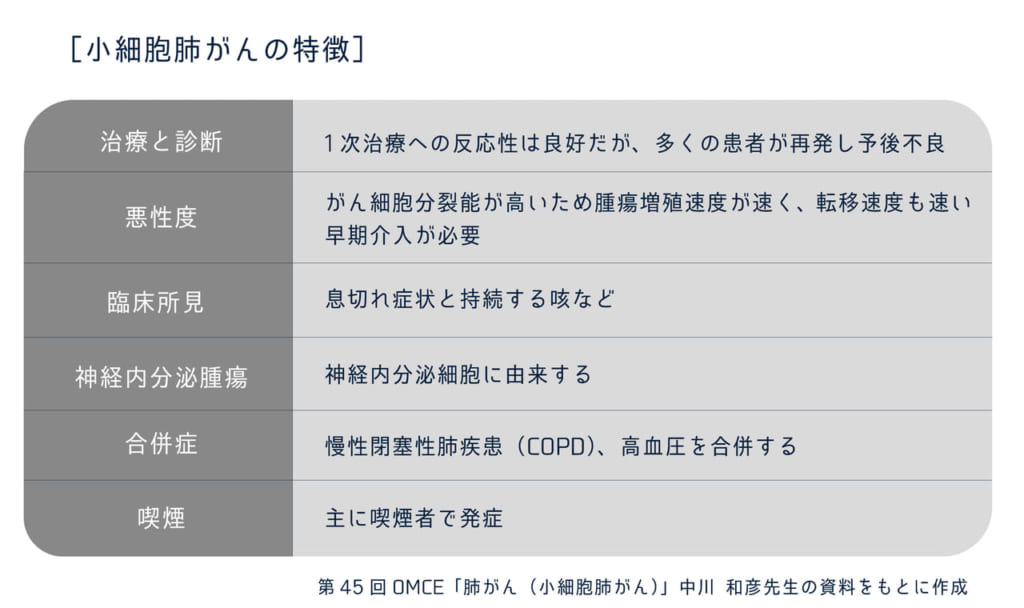
小細胞肺がんの基礎知識
今回は、肺にできた原発性の肺がんについてお話頂きました。
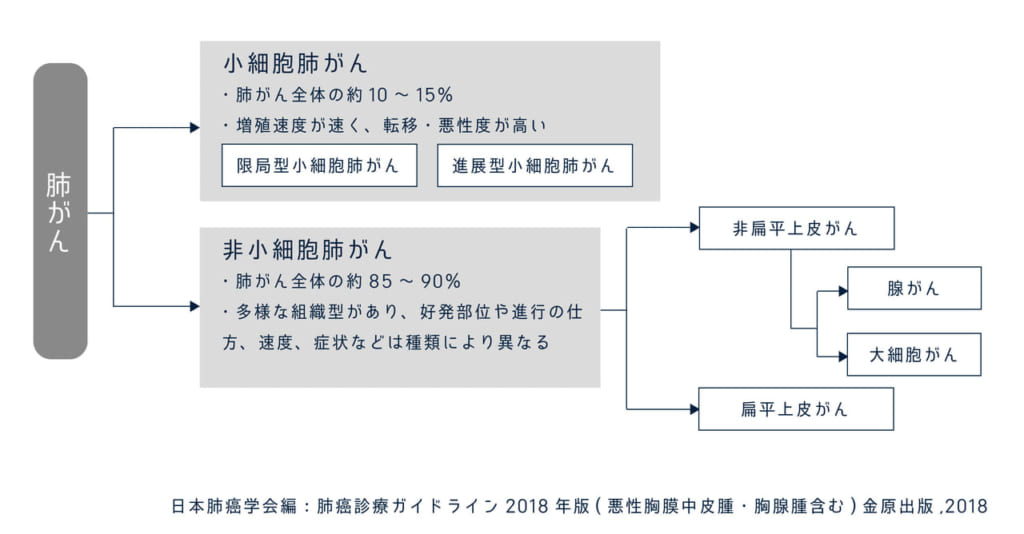
肺がんは、小細胞肺がんと非小細胞肺がんに分かれて、小細胞がんではない非小細胞肺がんは、扁平上皮がんと非扁平上皮がんに分かれて、非扁平上皮がんには腺がんと大細胞がんが含まれています。この非扁平上皮がんはアリムタという薬が適用になります。
小細胞肺がんは何かというと、病理的にみて特徴的なために分類されたものになります。小細胞肺がんは限局型と進展型に分けられます。
上皮性腫瘍の中に、腺がん・扁平上皮がん・神経内分泌腫瘍があり、その神経内分泌腫瘍の中に、小細胞がんがあります。
小細胞がんは核が非常に大きいというのが特徴です。また、神経内分泌腫瘍と言われ、神経細胞から出てきたがん細胞を言います。
もう一つの特徴が部位別で見た際に「肺門(中心)型」と分類されます。がんが肺の入り口付近(肺門)にでき、症状が出やすいと言われます。CTで見ると、縦隔リンパ節と一体となり、反回神経が麻痺することで、声がかれたり(嗄声)します。
症状で見ると、一番多いのは胸痛・食欲不振で、上大静脈症候群(上大静脈が潰され、心臓に血が戻ってこれなくなるので、首から上がうっ血し、腫れる)・ 側副血行路(血管が徐々に詰まっていく場合に、それを補うよう自然に発達してくる別の血流路のこと)ができるので、胸のあたりの静脈が怒張して見えるなどの症状も現れる事があります。
また、小細胞がんは腫瘍随伴症状がでます。腫瘍ができる事により、抗体ができるといわれ、それが様々な問題を引き起こし、特有な症状を引き起こします。
例えば、中枢性肥満(ムーンフェイスなど)などを引き起こすクッシング症候群、SIADH(抗利尿ホルモンが異常に産生され、低ナトリウム血症を来す疾患)、ランバート症候群(神経と筋肉との間での情報伝達を阻害し、筋力低下を引き起こす自己免疫疾患)、ふらつきや歩行困難を引き起こす小脳変性症などがあります。
また、予後を規定する特別な因子はありませんが、病期(ステージ)やPS(パフォーマンスステータス/全身状態や生活のアクティビティ)により決まります。どんな治療をするにしても、このPSは大切な判断となり、寝たきりの方などが抗がん剤治療をすると効果は下がり副作用が上がるため、治療をしない方が良いという判断になります。
また、いずれの病期においても、小細胞肺がんは5年生存率は高くありません。これは悪性度が高いという事を意味します。腺がんの5年生存率は10年前と比較し、かなり改善され、扁平上皮がんも少し改善されました。
しかし、小細胞肺がんはほぼ変わりません。
診断と治療については、疑われる人に病理学的な検査をすることが一番大切になります。何期であるか、限局型か進展型かなどを診断します。限局型は根治的な放射線治療の適用になります。
進展型であれば、化学療法を行います。次に血算(血液のデータ)や生化学検査をみて、全身の主要機能が保持されているかどうかという状態を確認します。
病期の分類として、限局型は原発の病変が同側内にあります。進展型は対側の肺門にすでにリンパ節転移があるような場合です。両方の肺門を含めて放射線を照射することは危険でリスクが高いので、できません。
また、胸水がたまっている場合も、根治的照射はできません。
まとめとして、次のようなことが言えます。
限局型小細胞肺がんについて
限局型小細胞肺がんの治療について、いくつかの臨床試験の結果を教えて頂きました。
結果は、
化学療法と放射線療法のどちらもやる併用治療を、同時に行い、なおかつ放射線療法は1日2回の分割照射で、併用のタイミングは早期にすることが勧められる
という結論が出ました。
更に、限局型小細胞肺がんの場合、予防的全脳照射というものがあります。これは、初回治療後の再発部位として脳転移が多いことから、再発を予防するために全脳照射を行うというものです。
まとめると、限局型小細胞肺がんの標準治療は、シスプラチン+エトポシド+胸部放射線治療(1.5Gyを1日2回、3週間トータル30回、総線量45Gy)の化学放射線療法を行います。
完全寛解であれば、予防的全脳照射が推奨され、治癒が期待される病態です。
進展型小細胞肺がんについて
進展型小細胞肺がんでは、1970年代のPE療法(シスプラチン+エトポシド)の2剤併用が開発され、その後大きな進歩はありませんでした。
しかし、今年は大きな飛躍の年と言われ、免疫チェックポイント阻害薬と抗がん剤の併用が有効であるという事が分かり、保険で認められました。(2019年/テセントリク+カルボプラチン・エトポシド療法が進展型小細胞肺がんに対しての効能・効果追加)
免疫チェックポイント阻害薬は、非小細胞肺がんでは画期的な薬と言われますが、早期ではがんが増大してしまうのではないかといった可能性や、長期生存する方もいますが、それは限定的である、といったような課題もあります。
そこで、抗がん剤と免疫チェックポイント阻害薬を併用するとこれらの課題が克服できるのではないか、という考えで、臨床試験が進んでいます。
小細胞肺がんに対する免疫チェックポイント阻害薬の疑問と今後の課題としては、どんな方が効きやすいのかというバイオマーカーが小細胞肺がんには現在ないこと、なぜ非小細胞肺がんと比較して有効性が低いのか、という事が挙げられます。
しかし、免疫チェックポイント阻害薬が小細胞肺がんに使用できる薬として追加されてきた、というのは大きな朗報です。これをより有効に使用するために、より様々な工夫を追求する必要があります、と先生は最後に語り、締めくくりました。
質問コーナでは「PD1阻害薬とPDL1阻害薬で効果が違うのはなぜか」「PDL1以外にも他の注目すべき要因はあるか」「遺伝子検査はどの病院でどんな患者さんが対象か」などの質問が寄せられました。
「PD1阻害薬とPDL1阻害薬で効果が違うのはなぜか」という質問には、両者の明確な差はあまり認めません。しかし、抗がん剤との併用の所では若干PD1抗体であるキイトルーダーの効果があまりにも良く、PDL1抗体のテセントリクを用いた4剤併用の試験(カルボプラチン・タキソール・アバスチン・テセントリク)との比較があまりよく見えませんでした。
様々な結果の「見え方」というものがあり、比較する相手が強力であると、効果が良く見えません。しっかり検討しないと実際にはどれ程の効果か判断できません。
薬剤を無再発生存期間の中央値を比較する、生存期間の中央値を比較する、観察期間の長さ、集められた集団の質など、様々な問題を検討する必要があります。
また、PDL1の方が肺臓炎などの副作用が少ないのではないかと言われていますが、これもまだはっきりと結果は出ていません。したがって、今のところはPD1阻害薬とPDL1阻害薬の両者をはっきり区別できるとはまだ言えません。
「PDL1の実用化など、様々なニュースが出てきているが、それに続く他の注目すべき要因はあるか」という質問には、2番目に来るのは、TMB(Tumor Mutation Burden/遺伝子変異数)という、遺伝子変異の数がいくつあるかという指標です。
TMBが沢山あるほど、免疫チェックポイント阻害薬が効きやすいのではないかと言われていますが、まだはっきりとはしていません。遺伝子スクリーニングで、国が承認したFoundation Oneでは、遺伝子変異のスクリーニングと一緒にこのTMBも出ます。
「遺伝子検査はどの病院でどの状況で、どんな患者さんが対象か。また、医療者側から進められるのか」という質問には、病院や医師次第になります。なぜかというと、病院や医師にかかる負担がとても大きいためです。
検体を国立がん研究センターに送る必要などがあり、また人員も多く必要で、とても大変な仕事になります。また、対象は標準治療が無くなる方ですが、その方が亡くなった場合、代金は病院の負担というリスクもあります。
更に、パネル検査を依頼する連携病院ですと、公的なサポートはなく、更にお金もかかります。メディアで期待を煽りますが、医師としっかり話しあう必要があるようです。
当日ご聴講された方々より、「わかりやすく、理解ができた」「単独のセミナーとして学べる機会が少ないので、大変参考になった」など、多くのご感想が寄せられました。
治療の進歩があまりなかった小細胞肺がんですが、希望の持てるニュースも含め、丁寧に分かりやすく教えて頂けました。中川先生、ご参加された皆様、本当にありがとうございました。